di Sergio Mauri
TENSIONE DI VAPORE
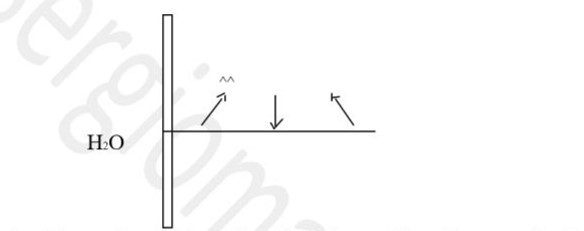
È la pressione del vapore in equilibrio con il suo liquido in un ambiente chiuso. Essa dipende dal liquido e dalla temperatura.
Questo equilibrio si crea quando la velocità di evaporazione è uguale alla velocità di condensazione, le quali a loro volta dipendono dalla probabilità del passaggio delle singole molecole da una fase all’altra.
La temperatura aumenta la probabilità del distacco delle particelle e quindi del passaggio fra liquido e vapore. Per questo motivo aumentando la temperatura aumenta la tensione (pressione) di vapore.
[La tensione è il contrario della pressione, è un risucchio].
Quando la velocità di un determinato fenomeno è uguale alla velocità del fenomeno inverso si ottiene una situazione di equilibrio dinamico: esiste una proprietà macroscopica il cui valore rimane costante (in questo caso la tensione di vapore), ma tale proprietà dipende dal comportamento delle particelle microscopiche, le quali continuano a modificare il loro stato.
Abbassamento della tensione di vapore.
La presenza di un soluto diminuisce la probabilità del passaggio allo stato di vapore da parte del solvente, infatti sappiamo che una parte delle particelle (molecole) di solvente è “vincolata” alle particelle di soluto.
Questo significa che la tensione di vapore diminuisce.
Numero di particelle.
Elemento chimico: insieme di atomi che hanno lo stesso numero di protoni (numero atomico).
Isotopo: insieme di atomi dello stesso elemento che hanno lo stesso numero di neutroni.
Ione: atomo con numero di elettroni diverso dal numero di protoni.
Anione: (ione negativo): atomo con numero di elettroni maggiore rispetto al numero di protoni.
Catione: (ione positivo): atomo con numero di elettroni minore rispetto al numero di protoni.
Simbolo
A q
X
Z
X simbolo dell’elemento
Z numero atomico
A numero di massa (somma di protoni e neutroni)
q carica elettrica